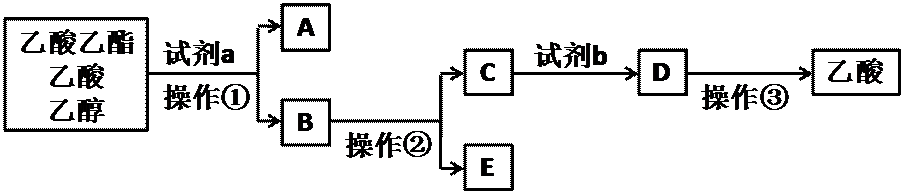- 乙酸的化学性质
- 共7题
8.某羧酸酯的分子式为C57H104O6,1mol该酯完全水解可得到1mol甘油
[HOCH2CH(OH)CH2OH]和3mol羧酸。该羧酸的分子式为
正确答案
解析
碳氢氧原子守恒,能得出答案A。
考查方向
解题思路
C57H104O6 + 3H2O →HOCH2CH(OH)CH2OH + 3 羧酸
易错点
忽略掉酯的水解需要水参加。
知识点
己二酸 
可能用到的有关数据如下:
实验步骤如下;I、在三口烧瓶中加入16 mL 50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。II、水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。III、当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止。IV、趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤得粗产品。V、粗产品经提纯后称重为5.7g。请回答下列问题:
27.仪器b的名称为__________。
28.向三口烧瓶中滴加环己醇时,要控制好环己醇的滴入速率,防止反应过于剧烈导致温度迅速上升,否则.可能造成较严重的后果,试列举一条可能产生的后果:_________________________________________________________________。
29.已知用NaOH溶液吸收尾气时发生的相关反应方程式为:2NO2+2NaOH=NaNO2+NaNO3+H2O NO+NO2+2NaOH =2NaNO2+H2O ;如果改用纯碱溶液吸收尾气时也能发生类似反应,则相关反应方程式为:_____________________________、________________________________。
30.为了除去可能的杂质和减少产品损失,可分别用冰水和 洗涤晶体。
31.粗产品可用 法提纯(填实验操作名称)。本实验所得到的己二酸产率为 。
正确答案
(1)球形冷凝管(或冷凝管)
解析
(1)冷凝管主要用来冷凝蒸汽。
考查方向
解题思路
(1)冷凝管的使用。
易错点
重结晶法。歧化反应。实验仪器的再认。产率计算。根据条件书写方程式。
正确答案
(2)反应液暴沸冲出冷凝管;放热过多可能引起爆炸;产生的二氧化氮气体来不及被碱液吸收而外逸到空气中。
解析
(2)应液暴沸冲出冷凝管;放热过多可能引起爆炸;产生的二氧化氮气体来不及被碱液吸收而外逸到空气中。
考查方向
解题思路
(2)当两种盐,它们的溶解度随着温度的变化,而不同时使用重结晶法。
易错点
重结晶法。歧化反应。实验仪器的再认。产率计算。根据条件书写方程式。
正确答案
(3) 2NO2+Na2CO3=NaNO2+NaNO3+CO2 NO+NO2+Na2CO3=2NaNO2+CO2
解析
(3)NO2与Na2CO3反应时,根据已知可以看出会发生歧化反应,所以有NaNO2和NaNO3生成,而碳的化合价不发生改变,以二氧化碳的形态出现。
考查方向
解题思路
(3)当碰到不熟悉的方程式时,观察题干给出的反应物与生成物,再利用得失电子守恒配平。
易错点
重结晶法。歧化反应。实验仪器的再认。产率计算。根据条件书写方程式。
正确答案
(4) 苯
解析
(4)用溶解性更好的有机溶剂洗涤效果会更好。
考查方向
解题思路
(4)洗涤产物时不能使之溶解。
易错点
重结晶法。歧化反应。实验仪器的再认。产率计算。根据条件书写方程式。
正确答案
(5)重结晶 75%
解析
(5)m(环己醇)=5.4 *0.962。再根据质量比进行计算。
考查方向
解题思路
(5)反应液暴沸冲出冷凝管;放热过多可能引起爆炸。
易错点
重结晶法。歧化反应。实验仪器的再认。产率计算。根据条件书写方程式。
10.现拟分离乙酸乙酯、乙酸、乙醇的混合物,如图是分离操作步骤流程图。下列有关说法错误的是
正确答案
解析
分离粗产品乙酸乙酯、乙酸和乙醇的混合物,加入饱和碳酸钠溶液,乙酸乙酯不溶于饱和碳酸钠,采用分液的方法即可,水层中的乙醇易挥发,可采用蒸馏方法分离,乙酸钠要用硫酸反应得到乙酸,再蒸馏得到乙酸;
操作①用到的玻璃仪器主要有分液漏斗、烧杯;工业制备无水E物质的方法是在E中加生石灰后进行操作②;试剂b可用硫酸;D.操作③是蒸馏操作而不是过滤操作的仪器。
考查方向
解题思路
乙酸乙酯、乙酸和乙醇的分离,最好先用饱和Na2CO 3溶液洗涤,这样首先分离出乙酸乙酯,而在洗涤液中留下CH3COONa和乙醇,再用蒸馏的方法蒸出乙醇,最后把CH3COONa转化为CH3COOH再蒸馏,即可得到CH3COOH。
易错点
本题考查物质的分离与提纯,题目难度中等,注意分离混合物的操作步骤。
知识点
关于某有机物 
正确答案
解析
略
知识点
26.乙醛能与银氨溶液反应析出银。如果条件控制适当,析出的银会均匀地分布在试管壁上,形成光亮的银镜,这个反应又叫银镜反应。银镜的光亮程度与反应条件有关。某课外活动小组同学在课外活动中对乙醛的银镜反应进行了探究。
Ⅰ. 探究银镜反应的最佳实验条件部分实验数据如下表:
请回答下列问题:
(1)读表若只进行实验1和实验3,其探究目的是 _________________ 。
(2)推理当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11时,出现银镜的时间是__________;要探索不同水浴温度下乙醛进行银镜反应的最佳条件,除了测量银镜出现的时间外,还需要比较不同条件下形成的银镜的__________ 。
(3)进一步实验 若还要探索银氨溶液的用量对出现银镜快慢的影响,如何进行实验?
Ⅱ. 探究对废液的回收处理:
银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环境,且造成银资源的浪费。通过查找资料,已知从银氨溶液中提取银的一种实验流程为:
操作④的方法是:把Ag2S和铁粉放到烧杯中加浓盐酸搅拌煮沸,使Ag2S变成银粉。反应的化学方程式为:
(4)若获得的银粉中含有少量没有反应完的铁粉,除去铁的反应的离子方程式为:
__________,需要用到的玻璃仪器有__________(填编号)。
(5)操作④应在(填实验室设备名称)__________ 中进行。
(6)要洗去试管壁上的银镜,采用的试剂是__________(填名称)。
正确答案
见解析。
解析
(1)比较乙醛用量不同时生成银镜的时间
(2)在6.5~9min之间;光亮程度
(3)保持其他的实验条件不变,改变银氨溶液的用量,测量生成银镜的时间
(4)Fe+2H+==Fe2++H2↑;b e f
(5)通风橱
(6)硝酸
知识点
下列各组有机物只用一种试剂无法鉴别的是
正确答案
解析
略
知识点
7.关于醋酸的下列说法不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析